Medicina personalizada e o futuro do seu bem-estar
Nos últimos dois séculos os avanços científicos transformaram os tratamentos médicos e, como resultado das melhorias da saúde, expectativa e qualidade de vida cresceram consideravelmente. Nosso sistema atual, no entanto, ainda possui algumas deficiências, sendo duas bastante relevantes: diagnósticos lentos ou incorretos e tratamentos que não consideram a individualidade de cada organismo.
Isto acontece porque a medicina de hoje funciona com base em "padrões de cuidado", que são determinados pela média das respostas em grandes cortes. Dessa forma, a teoria é que todos deveriam receber o mesmo cuidado com base em ensaios clínicos. Porém, isso não corresponde à realidade, e cada organismo funciona de uma maneira bastante particular. Essa é uma lacuna que a tecnologia de medicina personalizada buscará atender.
Ciência e tecnologia em busca da saúde
Por meio de ferramentas mais precisas, médicos poderão selecionar tratamentos individualizados, baseados no perfil molecular de um paciente, minimizando efeitos colaterais prejudiciais e oferecendo tratamentos mais eficazes. A medicina personalizada possibilita uma visão global do indivíduo, considerando suas características próprias. Trata-se de uma abordagem multifacetada, em que o paciente não será apenas diagnosticado e tratado, e que possibilita detectar doenças em fases anteriores, aumentando as chances de cura.
O conceito de medicina personalizada engloba: testes genéticos para revelar predisposição a doenças; intervenção no estilo de vida para prevenção; detecção precoce da doença no nível molecular; diagnóstico preciso e estratégia de tratamento customizada; resultados melhorados através de tratamentos em alvos pré-selecionados com redução de efeitos colaterais; e monitoramento ativo de resposta ao tratamento e progressão da doença.
Portanto, a medicina personalizada seria um conceito que engloba idade, sexo, altura, peso, dieta, estilo de vida, ambiente de trabalho, histórico familiar, entre muitos outros. Hoje, já consideramos o histórico familiar para a prevenção de doenças, como diabetes ou colesterol, por exemplo, e isso deve ir além, já que avanços científicos oferecem o potencial para definir o risco de um indivíduo com base em sua constituição genética.
Enquanto os campos de pesquisa translacional estudam a contribuição de genes, proteínas e vias metabólicas que podem levar à suscetibilidade de doenças, a farmacogenética examina o impacto da variação genética na resposta aos medicamentos. Com a combinação desses dois campos, espera-se que surjam novas abordagens para diagnóstico, desenvolvimento de medicamentos e terapia individualizada.
Algumas pedras no caminho
É claro que avançar em estudos ligados ao DNA não é algo simples. Mesmo que hoje os exames genéticos sejam mais acessíveis ao público graças a uma expressiva redução de custos nos últimos 10 anos, a maioria dos médicos ainda não está qualificada para compreender os testes genéticos e muito menos para comunicar os resultados com precisão aos seus pacientes.
Erros de interpretação desses exames são bastante comuns, segundo médicos geneticistas, e esses equívocos podem causar problemas sérios. Um estudo de 2012 na publicação científica The Cancer Journal, por exemplo, descreve o caso de uma mulher que foi submetida a cirurgias extremas, incluindo a remoção de seu útero, devido a uma leitura incorreta de seus resultados do teste genético.
Em muitos casos, essa falta de conhecimento ocorre porque muitos médicos em atuação se formaram antes que o genoma humano fosse sequenciado. Especialistas em genética poderiam preencher essa lacuna, porém nós sabemos bem que muitos lugares sofrem com a deficiência de médicos generalistas ou de especialistas, como cardiologistas ou oncologistas. Daí a conseguir acesso a um especialista em genética é um salto muito grande.
Como todo novo conhecimento, há uma curva de aprendizado. Possivelmente, em poucos anos nossos médicos estarão mais preparados para entender e nos explicar resultados complexos de genética. Há um bom caminho pela frente.
Armas contra todas as doenças, até o câncer
A Moderna Therapeutics, empresa de biotecnologia de Boston, é uma das poucas que desenvolvem tecnologias para transformar as próprias células das pessoas em fábricas de medicamentos usando RNA mensageiro, ou mRNA. Por meio dessas transformações, é possível convencer o corpo a produzir substâncias químicas que matam o câncer, proteínas que curam problemas no coração ou anticorpos que "caçam" vírus.

Além dos programas que a Moderna tem para doenças infecciosas, doenças cardiovasculares e doenças raras, talvez nada tenha atraído tanto a atenção como a ideia de criar drogas únicas contra o câncer. A empresa inicia o processo de fazer cada tratamento individualizado com um par de perfis genéticos retirados de um paciente com câncer. Um vem de uma gota de tecido tumoral, um de um frasco do sangue. Ao comparar os dois, um algoritmo vasculha as mutações que causaram esse câncer em particular.
Ao mesmo tempo, outro algoritmo produz uma lista de 20 alvos proteicos que ele prevê que ensinarão o sistema imunológico a atacar o tumor, com base nessas mutações. Outro projeta a série de nucleotídeos que as máquinas automatizadas vão montar em um medicamento de RNAm. Trabalhadores humanos monitoram o processo a partir de uma estação de trabalho e executam verificações de controle de qualidade, enquanto as máquinas fazem a maior parte do trabalho.
A startup americana não é a única que trabalha com essa possibilidade. A alemã BioNTech já iniciou os ensaios da Fase 1/2 para sua vacina contra o câncer individualizada em pacientes com múltiplos tumores com seu parceiro, a Genentech. A CureVac, também com sede na Alemanha, estabeleceu a primeira instalação de fabricação de GMP para mRNA em 2006 e hoje têm três programas de vacinas contra o câncer atualmente em testes clínicos.
A genômica não é tão simples assim
Uma vacina que cure o câncer parece mágica, e é uma busca de empresas e especialistas, porém a genômica oferece complexidades que são obstáculos a esse milagre. Hoje, os médicos sequenciam os genes das células cancerígenas e as comparam com células hospedeiras normais, uma tecnologia chamada genômica do câncer. Com o conhecimento a respeito do câncer, é possível personalizar o tratamento. Em tese, com algumas drogas utilizadas na medicina de precisão, e se um paciente tem uma mutação específica, é possível em combinação com quimioterapia, radiação ou cirurgia, curar o câncer ou torná-lo uma doença crônica como o diabetes.

Não há um consenso a respeito dos tratamentos para alguns tipos específicos de câncer, o que abre espaço para discussões e diversas opções de tratamentos. Ainda hoje existem poucos dados a respeito da doença, já que o primeiro câncer foi sequenciado apenas em 2006. Ainda sabe-se pouco a respeito das causas de muitos tumores, como os que atingem o cérebro, por exemplo.
Trilhões de bactérias e possibilidades
Seu microbioma é a coleção exclusiva de trilhões de microrganismos no seu corpo que têm um papel fundamental em seu bem-estar. Nossa pele, nossa boca e nosso intestino estão repletos de bactérias responsáveis por uma vida saudável ou doenças. A startup uBiome utiliza aprendizado de máquina, inteligência artificial, estatísticas avançadas e um processo de sequenciamento de precisão para analisar os micróbios de seus clientes.
O procedimento é simples: o usuário recolhe sua amostra para o laboratório com um kit totalmente pronto. A uBiome utiliza seus métodos para analisar as bactérias e envia um link seguro para que o usuário baixe os resultados de testes. O cliente pode colher uma amostra do intestino e obter uma análise detalhada de seu microbioma para compreender como ele está funcionando. Há também a opção de recolher várias amostras intestinais, para ver como o microbioma muda com o tempo.

Por meio dos resultados do teste, o paciente pode realizar mudanças em sua alimentação e estilo de vida para combater as bactérias ruins ou fortalecer as bactérias boas presentes em no organismo. A empresa também trabalha em parceria com médicos, que podem solicitar o exame e, assim, trabalhar de forma individualizada com os resultados e possibilidades de tratamento.
Formado por bactérias, vírus, fungos e outros micro-organismos que podem ser benéficos para a saúde humana, o microbiano desequilibrado afeta a saúde da pele, causando acne, eczema, rosácea, entre outras condições. A startup atua em parceria com grandes empresas, como a L'Oréal, para compreender o microbioma da pele e sua importância como barreira de proteção. Por meio dessa parceria, as duas pretendem conduzir novas pesquisas sobre o ecossistema bacteriano da pele.
Theranos e o escândalo regulatório da década
A Theranos parecia ter um serviço perfeito: oferecer facilidade nos exames de sangue, sem dor, sem a necessidade de um enfermeiro e sem sujeira. A empresa prometia testes com apenas um pequeno furinho no dedo e poucas gotas de sangue. O serviço, no entanto, se provou bom demais para ser verdade, foi acusado de fraude e encerrou suas atividades.
Um dos fatores interessantes é que sua fundadora, Elizabeth Holmes, apoiava o aumento da regulamentação de sua indústria. Em um artigo de 2015, a empresária pedia a supervisão do Food and Drug Administration (FDA) sobre todos os testes desenvolvidos em laboratório. Essa teria sido uma estratégia de marketing ou fruto da sua alta confiança na tecnologia?

A partir deste episódio, muito se discute a respeito das deficiências da supervisão do FDA sobre testes laboratoriais. A agência atua melhor quando regula um "artifício" e não um serviço ou a prática da medicina. Por isso, quando se trata de diagnósticos como a plataforma de testes de sangue que a Theranos desenvolveu, o FDA se concentra principalmente nas ferramentas, e não na conduta do laboratório, ou em como os vários aspectos de um serviço de diagnóstico são executados.
São dois desafios grandes: construir uma boa plataforma de testes e executar um laboratório, sendo que a Theranos teve problema com ambos. Isso dificulta o trabalho do FDA. Atualmente, os reguladores do Medicare já inspecionam e supervisionam os serviços laboratoriais como parte das Clinical Labs Improvement Amendments (CLIA), um conjunto de normas regulatórias federais que se aplicam a todos os testes laboratoriais clínicos realizados em humanos nos EUA, exceto ensaios clínicos e pesquisa básica. Aqueles que defendem um exame mais rigoroso dos testes de laboratório argumentam que a FDA deve supervisionar os diagnósticos, não a CLIA, e regulá-los como dispositivos médicos, não como um serviço.
Além da Theranos, diversas outras startups estão buscando atingir diagnósticos complexos com processos e equipamentos simplificados. A empresa Genalyte é uma das que buscam atingir o que a Theranos não conseguiu. O FDA promete ser mais rigoroso com os testes que vêm a seguir.
Suplementação sob medida
A deficiência de vitaminas também pode ser solucionada por meio da medicina personalizada. A Baze oferece um serviço de vitaminas sob medida com base em um teste de sangue caseiro. Com o kit de teste enviado pela empresa, o cliente recolhe a amostra e envia de volta. Com uma série de testes, determina-se sua deficiência de vitaminas e você as recebe em casa. Outras empresas, como Persona e Vous, também oferecem serviço de vitaminas personalizado, mas usando como base dados demográficos e respostas a questionários, não testes fisiológicos reais.
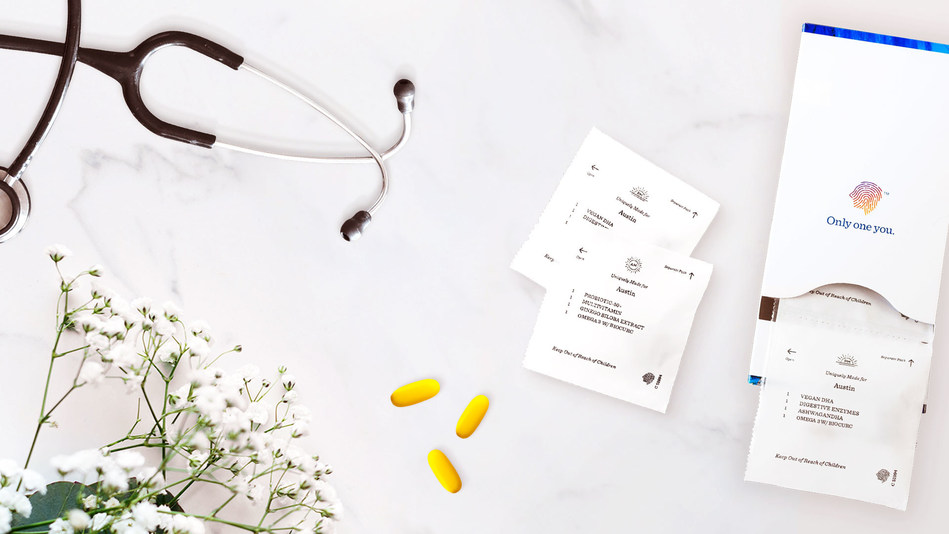
Pode parecer estranho fazer uma exame de sangue em casa, sem que um profissional da saúde te auxilie. O sistema da Baze é baseado em um novo dispositivo chamado TAP, em que o paciente o pressiona contra o corpo e empurra um botão na parte superior. Isso leva uma coleção de microagulhas à pele, atraindo uma pequena quantidade de sangue – apenas 100 microlitros – para dentro de suas entranhas. A partir daí o cliente recebe seus resultados e os pacotes de vitaminas adequados às suas necessidades.
Mas será que os testes clínicos do Baze são realmente eficazes? O teste lembra bastante o caso de Theranos, embora o fundador do Baze garanta que o trabalho do teste TAP foi publicado na revista especializada Nature, e tenha autorização da FDA como um dispositivo médico do tipo II. O assunto, no entanto, é tema de longas discussões entre médicos.
A regulamentação desse tipo de tecnologia para o uso da medicina personalizada não deve ser um problema simples de resolver. Porém, não existem dúvidas de que a medicina personalizada fará parte do futuro de todos nós. A mudança progressiva deve tomar conta dos consultórios ao longo dos anos, com o avanço de tecnologias que possibilitam essa visão individualizada do paciente e de suas necessidades. É difícil prever, no entanto, se estas tecnologias estarão realmente disponíveis a todos, já que sabemos da existência de muitas deficiências nos sistemas de saúde ao redor do mundo e da imensa dificuldade da democratização do acesso à saúde.













ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.