A superação do câncer está mais próxima do que você imagina
Novos e mais personalizados diagnósticos para o câncer. Pesquisas com prazos mais curtos e para condições raras. Mais assertividade e menos efeitos colaterais nos tratamentos medicamentosos para além da quimioterapia. Estes são apenas alguns dos benefícios que a nova tecnologia de mapeamento genético completo promete. Uma profunda mudança de paradigma no diagnóstico e tratamento de cânceres pode nos ajudar a viver mais e melhor.

O caminho do tratamento hoje
Se uma pessoa possuir uma suspeita de câncer, ela é levada a fazer exames de analises clinicas e também de imagem, tomografias e ressonâncias magnéticas. A partir destes exames, ela pode ser encaminhada para uma extrair uma biópsia. No procedimento, uma parte do tecido do tumor é retirado e analisado em um laboratório por patologistas. O profissional irá avaliar as características deste grupo celular e determinar se o tecido é canceroso ou não, baseado em alguns parâmetros histológicos, como o formato das células e também na quantidade de núcleos que o tecido apresenta.
A partir da confirmação do diagnóstico, o paciente então é mais comumente submetido a radioterapia, quimioterapia convencional ou uma combinação de ambos, a depender do estágio, órgão em que se manifestou e prognóstico da doença. A quimioterapia é uma terapia que causa diversos efeitos colaterais, sendo eles mais de 40 tipos. Pesquisas indicam que cerca de 25% dos pacientes respondem bem ao tratamento. No entanto, a imensa maioria acaba sem outras opções para tratar sua condição, não tendo um tratamento personalizado e estando mais longe de uma potencial cura.
Até pouco tempo atrás, o câncer era considerado uma patologia que atinge um determinado órgão, e mais adiante passou a ser considerado com as análises dos tecidos uma doença que acomete as células. A partir de 2014, com a comercialização dos testes genéticos, o câncer passa a ser tratado como uma doença genômica. Isso quer dizer que o câncer é agnóstico com relação ao local e tipo de célula e sendo tratado no corpo todo, com terapias-alvo que ataquem o câncer orientados pelo perfil genético, existem mais chances de superar a doença.
Da biologia molecular para a medicina personalizada
As técnicas da biologia molecular aliadas com uma maior capacidade e menor custo para se fazer análise de dados faz com que a medicina personalizada já seja uma realidade. O sequenciamento genético de humanos, que começou como um projeto de pesquisa iniciado por Craig Venter e financiado pelo governo americano na década de 1900, à época custou cerca de 2,7 bilhões de dólares. Hoje, o mesmo processo custa cerca de 1000 dólares. A queda exponencial do custo e do tempo de processamento possibilitou uma série de análises mais complexas, e associação de genes a determinadas doenças, como o câncer.

O sequenciamento é realizado em equipamentos como o Illumina HiSeq 2000. Após rastreamento de características do câncer há o processamento de dados por plataformas e equipes de bioinformática para correlacionar e interpretar os dados. É necessário cruzar os dados do paciente em questão com bases de dados pré-existentes de outros pacientes para obter melhores evidências e entender os possíveis prognósticos da doença. A tecnologia permite entender quais marcadores tumorais estão relacionados a quais tipos de câncer. Um dos maiores bancos de dados do mundo pertence à americana Flatiron Health, baseada em Nova Iorque, que trabalha em parceria com hospitais, universidades e clínicas e possui mais de 260 mil perfis genéticos individuais, além de vasta literatura médica atualizada.
A análise dos sequenciamento ainda exige muita mão de obra especializada, como médicos geneticistas, oncologistas, biólogos moleculares. Visando automatizar as análises genéticas o hospital Albert Einstein, de São Paulo, criou a plataforma VarStation. A plataforma pode apoiar painéis germinativos, somáticos e também exomas – análises completas do DNA. Além de fazer parte das rotinas de análise dos laboratórios de Análises Clínicas do Albert Einstein, outros usuários podem usar a ferramenta e têm total controle e transparência dos parâmetros. A plataforma ainda conta com auditoria e segue as diretrizes do College of American Pathologists (CAP).
O caso Angelina Jolie – o teste germinativo
Um dos casos mais polêmicos e populares de intervenção médica após um diagnóstico advindo de um teste genético é o caso de Angelina Jolie. Após realizar um teste genético em que um marcador tumoral hereditário para o câncer de mama foi identificado, a atriz americana decidiu se submeter a uma dupla mastectomia preventiva, procedimento em que ambas as mamas foram removidas. A intervenção radical se deu pelo fato de que havia uma altíssima probabilidade de ela viesse a manifestar a doença que já tinha levado outras mulheres de sua família à morte.
Embora a escolha de Angelina tenha se tornado muito conhecida e até desejada por outras pessoas com parentes próximos com câncer, esta alternativa não seria recomendável para a maioria das pessoas. O teste que a atriz realizou é um exame que determina a origem germinativa dos genes, ou seja, quais genes foram herdados dos pais. Porém, a maior parte dos cânceres não têm origem hereditária e são desenvolvidos ao longo da vida. Muitas vezes o câncer parte de uma mutação de uma única célula, que então se espalha para outras e para outros tecidos.

Existe também um consenso entre pesquisadores de que fatores ambientais estão relacionados com o surgimento da doença. Hábitos, alimentação, exposição a agentes químicos, entre outros fatores estão entre os mais prováveis ligados ao desenvolvimento de cânceres. Algumas relações já estão mais claras: o uso prolongado de cigarros está diretamente ligado ao câncer de pulmão, língua, boca e garganta.
Para os tumores de tireóide, por exemplo, menos de 2% dos pacientes que apresentam uma lesão maligna herdaram os genes que causam a doença. Para conseguir detectar estes tipos de câncer, pode ser realizado um teste genético somático, que é uma impressão do perfil genético atual da pessoa, com todas as principais mutações ligadas ao câncer. É possível detectar mais de 400 genes relacionados ao câncer e se espera que este número cresça nos próximos anos com o avanço das pesquisas.
Detecção e tratamento através do perfil genético tumoral
Os testes da empresa Foundation Medicine, ligada ao grupo do laboratório farmacêutico suíço Roche, auxiliam na tomada de decisão de oncologistas e indicam opções de tratamento direcionado para alterações genômicas. São mais de 15 medicamentos oncológicos já disponíveis no mercado brasileiro e mais de 100 em estudo. O laboratório já vem desenvolvendo fármacos com base em perfilamento genético desde 1998. A Roche criou um dos primeiros medicamentos do mundo com ação citotóxica para o câncer de mama em uma parte específica do tumor orientados pela mutação genética HER2.
A assinatura genômica abrangente também pode auxiliar na prescrição de tratamentos mais eficazes para cada paciente e cada tipo de câncer. Muitos têm recorrido à imunoterapia como forma alternativa de tratamento, mas poucos têm obtido sucesso. A imunoterapia utiliza medicamentos que "reprogramam" e recrutam o sistema imunológico do paciente para combater o câncer. No entanto, estudos mostram que apenas 30% das pessoas respondem bem ao tratamento. Algumas possuem um gene que quando expresso determina resistência a este tipo de solução. Um teste genético somático poderia revelar esta informação e ajudar a equipe médica a decidir pelo melhor caminho logo no início do diagnóstico, o que aumenta as chances de sobrevida do paciente e remissão da doença.

No Brasil, já existem diversos laboratórios que realizam os testes de perfil genético tumoral. O que oferece o maior número de possibilidades de exames é o Fleury, através de sua unidade Fleury Genômica Oncologia. Os testes são pouco invasivos e realizados com uma única amostra de tecido tumoral ou de sangue, caso o paciente não tenha tecido ou não seja possível coletá-lo.
No Brasil, existe um programa que subsidia em até 90% o teste de perfil genômico compreensivo para quem não tem condições de pagar pelo exame. O valor do exame está em torno de 10 mil reais. Após a solicitação do médico para a realização, a análise de critérios socioeconômicos pode ser acionado via Concierge da Foundation Medicine, por telefone. Só em 2018, 875 pacientes se beneficiaram do programa.
Participar de estudos clínicos: por quê?
Para além do diagnóstico e tratamento, a abordagem de medicina personalizada na pesquisa oncológica, pode auxiliar a reduzir o tempo de pesquisa de novos medicamentos em estudos clínicos. O estudo clínico é a última fase de experimentos no desenvolvimento de novos fármacos, aquele que é testado em pacientes que podem se beneficiar do tratamento. O processo completo de criação de um novo fármaco pode ser pode levar até 10 anos e a parte do teste clínico, ou teste de estágio três, pode levar de 2 a 3 anos.
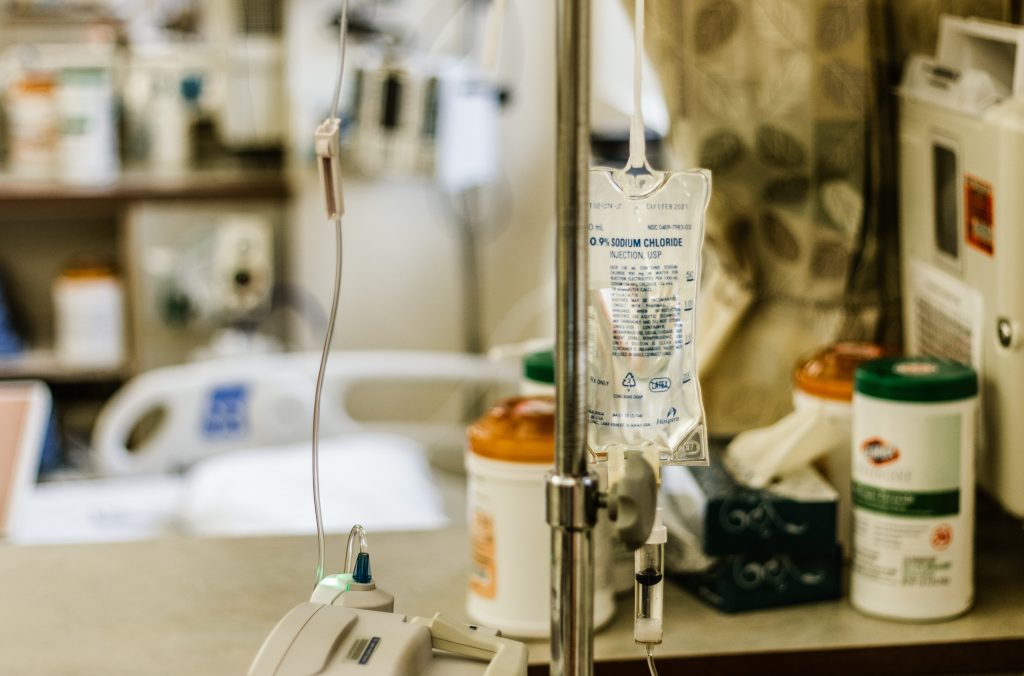
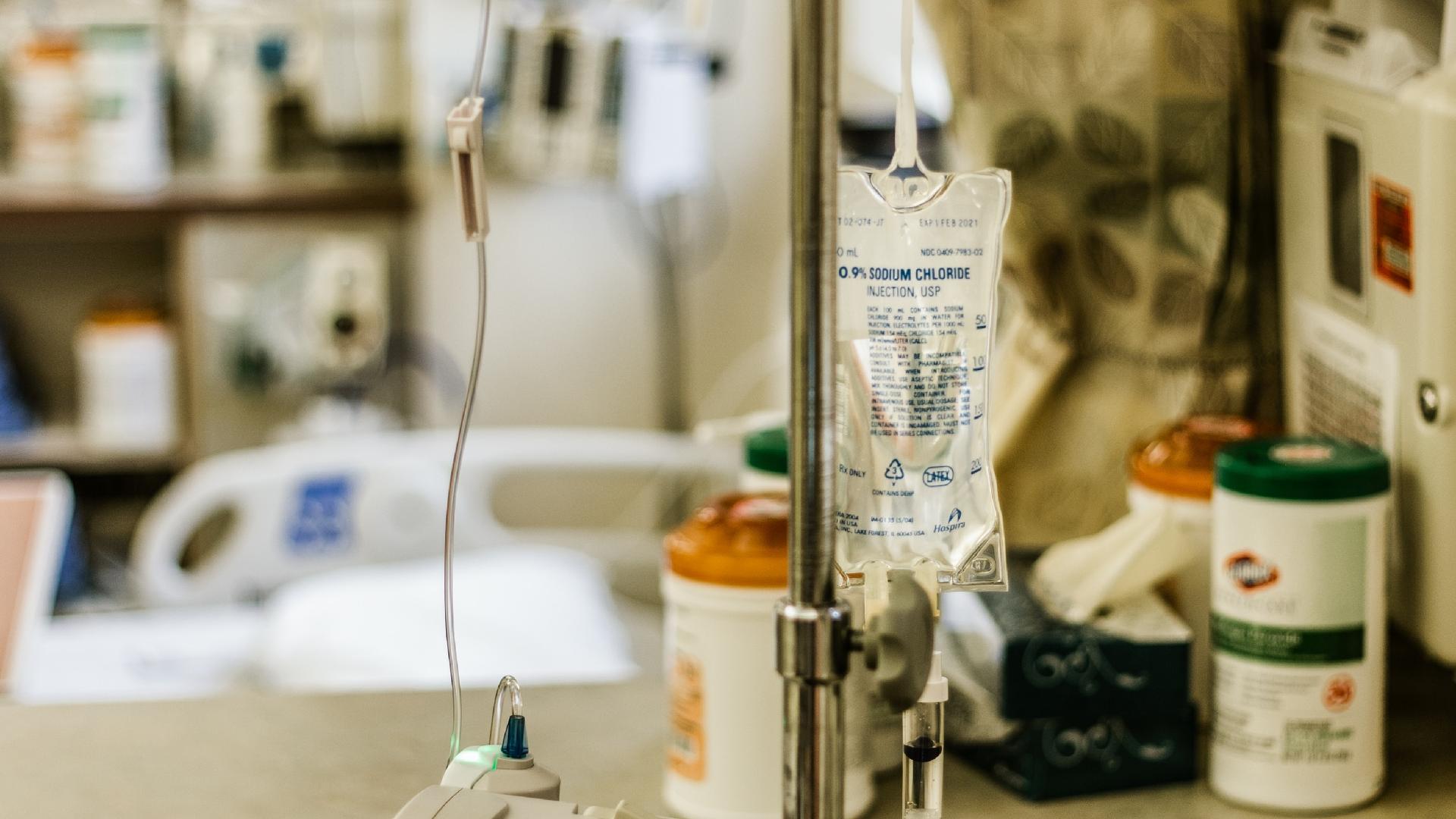
Para um paciente, participar de um estudo clínico pode parecer arriscado, porém apresenta grandes vantagens, se este paciente estiver em uma fase delicada do tratamento em que não haja resposta ou se detectar alguma mutação que está associada à baixa responsividade dos medicamentos que existem atualmente. Um estudo clínico, muitas vezes, dá acesso ao paciente a uma droga que iria só chegar ao mercado anos depois do estudo ser concluído. Quando se está enfrentando uma doença agressiva como o câncer, o estudo clínico pode ser uma das últimas esperanças de uma paciente e de sua família.
Um dos cânceres mais difíceis de serem tratados, é o câncer de origem primária desconhecida. Um estudo clínico oncológico para este tipo de condição, chamado de CUPISCO, está sendo realizado em mais de 23 países, como Áustria, Irlanda, Noruega também Brasil. No Brasil os testes estão conduzidos no ICESP (São Paulo), INCA (Rio de Janeiro) e no Hospital Conceição (Porto Alegre). No Hospital de Câncer de Barretos há um programa pioneiro para ser lançado em breve, mas ainda sem informações oficiais. Diversos outros testes em todo o mundo são realizados por laboratórios farmacêuticos com parceiros locais. No entanto, para participar é preciso estar ciente de todos os riscos associados e passar por uma triagem para participar. O oncologista é o profissional mais recomendado para fornecer orientação e que pode auxiliar o paciente sobre como encontrar e se inscrever em um estudo clínico para sua condição específica.













ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.